中国药品注册审评制度经历了一系列深刻改革,旨在鼓励创新、提高药品质量、加速新药上市。这一系列改革,如上市许可持有人制度(MAH)的全面实施、优先审评审批通道的建立、以及与国际接轨的审评标准提升,不仅重塑了药品研发与注册的生态,也为药品技术转让这一传统业务领域带来了全新的发展格局。技术转让,作为药品生命周期中优化资源配置、加速产品商业化的重要环节,正站在机遇与挑战并存的关键路口。
一、 改革带来的历史性机遇
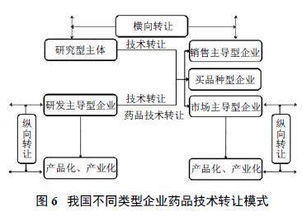
- 制度松绑,激活市场活力:MAH制度的推行是核心机遇。它实现了药品上市许可与生产许可的“解绑”,允许研发机构、科研人员等持有药品批文,并委托生产企业进行生产。这极大地降低了技术持有方进行转让的门槛和风险,使得更多实验室阶段的创新成果能够通过技术转让路径,快速找到具备生产能力和市场渠道的合作伙伴,实现产业化。技术转让不再必然伴随生产线的整体出售,变得更加灵活多样。
- 价值重估,创新成为硬通货:审评改革强调临床价值,对真正具有创新性、能够解决未满足临床需求的药品开辟了优先审评、突破性治疗药物等加速通道。这使得具有突出临床优势的早期项目或专利技术在转让市场上的价值显著提升。买方更愿意为具有明确创新点和市场潜力的技术支付溢价,激励了源头创新,也促使技术转让更早地介入研发链条。
- 路径清晰,降低转让不确定性:改革后的审评流程更加透明、可预期,技术要求与国际逐步接轨。这使得在技术转让过程中的尽职调查更有依据,对技术的成熟度、合规性、知识产权状况的评估更为准确。清晰的法规框架降低了交易双方因政策变动带来的不确定性,有利于达成更公平、稳定的转让协议。
- 生态繁荣,催生专业服务需求:随着交易活跃度提升,围绕药品技术转让的第三方专业服务市场,如法规咨询、价值评估、知识产权服务、交易中介等,迎来发展契机。一个更加专业、细分的服务体系能够进一步促进技术的高效流转。
二、 面临的全新挑战
- 标准提升,对技术质量要求更严苛:与国际接轨的审评标准,意味着转让的技术必须满足更高的药学、临床和质量一致性评价要求。一些基于旧标准开发、数据不够完整或质量体系有缺陷的技术,其转让价值将大打折扣甚至无法转让。这对技术持有方的研发质量和数据管理能力提出了严峻挑战。
- 责任明确,MAH制度下的风险管控:在MAH制度下,上市许可持有人对药品的全生命周期质量承担主体责任。对于技术受让方(尤其是成为MAH的一方)而言,如何确保对受托生产企业的有效管理,如何建立覆盖全链条的质量管理体系,是全新的课题。技术转让协议中关于质量责任、药物警戒、上市后研究等责任的划分必须极其清晰。
- 竞争加剧,对综合研判能力要求更高:政策鼓励创新导致源头项目争夺激烈,优质技术成为稀缺资源。潜在受让方(如大型药企)的选择也更多,其眼光更加挑剔。技术转让的成功不再仅依赖于“有批文”,更取决于对技术临床优势、市场潜力、专利布局、后续开发成本与风险的精准综合研判。这对交易双方的战略眼光和专业能力构成了挑战。
- 过程复杂,全链条整合需求凸显:现代药品技术转让往往不是简单的“纸面资料”移交,而可能涉及生产工艺的转移与验证、质量标准衔接、供应链重构、注册档案的变更与申报等一系列复杂活动。这要求交易双方具备强大的项目管理和跨部门整合能力,任何环节的疏漏都可能导致转让失败或成本超支。
三、 展望与应对之道
面对机遇与挑战,药品技术转让的参与者需要积极适应新环境:
- 对于技术持有方:应注重研发的合规性与数据完整性,加强知识产权保护与布局,在研发早期就引入商业化思维,提前准备符合新规的技术转让资料包。
- 对于技术受让方:需建立科学的技术评估体系,不仅关注眼前批文,更要评估技术的长期开发潜力和MAH责任下的风险管控能力,加强自身对委托生产的管理体系建设。
- 对于行业整体:应倡导更加规范、诚信的交易文化,发展专业的中介评估机构,利用合同明确界定各环节权责利,共同构建一个高效、透明、风险可控的药品技术转让市场。
中国药品注册审评制度改革如同一股强劲的东风,既为药品技术转让打开了更广阔的空间,也设定了更高的航行标准。唯有那些能够深刻理解政策内涵、精准把握技术价值、并具备卓越执行力的企业与机构,才能在这场变革中乘风破浪,实现技术与资本、研发与市场的成功对接,最终惠及患者,推动中国医药产业的高质量发展。